高校化学で20種類ものアミノ酸を習い、
大変な思いをしていませんか?
さらには4種類もの検出反応が登場し、
混乱している人も多いでしょう。
この記事ではアミノ酸の性質・検出反応をまとめました。
ここの内容を最後まで読むことで、
アミノ酸の本質的な性質を理解することができ、
4種類の検出反応を確実に見分けられるようになります。
今回は以下の流れで解説していきます。
目次
アミノ酸とは

「アミノ酸」とは、
カルボキシ基-COOHとアミノ基-NH2を、
両方持っている有機物のことです。
その中でも特に、
-COOHと-NH2が同じ炭素にくっつくものを、
「α-アミノ酸」と言います。
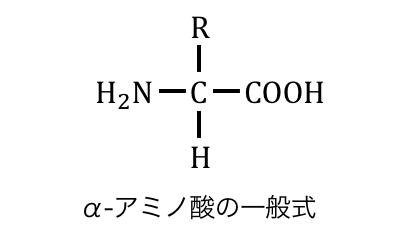
α-アミノ酸はこの-Rが変わることで、
約20種類があります。
本記事ではα-アミノ酸の性質を解説しますが、
20種類の化学式の覚え方は以下で解説しているので、
ぜひそちらも参考にしてみてください。
アミノ酸の性質
アミノ酸には面白い性質がいくつもあります。
順番に確認していきましょう。
酸性アミノ酸・塩基性アミノ酸
-COOHと-NH2を持っていますが、
通常α-アミノ酸はおおよそ中性です。
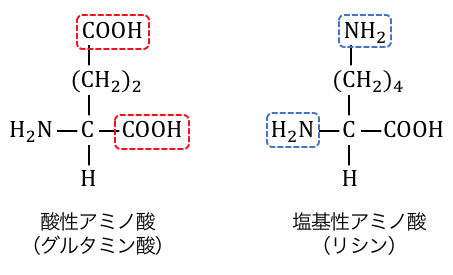
しかし-Rに-COOHを含む場合は酸性となり、
そのようなアミノ酸を「酸性アミノ酸」といいます。
同様に-Rに-NH2を含むものを「塩基性アミノ酸」といいます。
光学異性体の存在
アミノ酸の基本構造を見ると、
中心の炭素が不斉炭素原子になっていることがわかります。
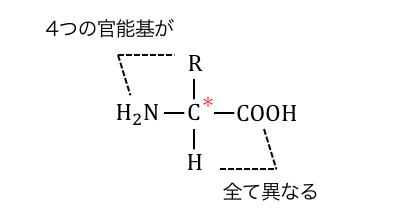
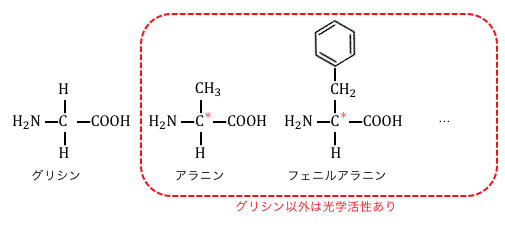
ただし-R=-Hである「グリシン」のみは、
不斉炭素原子を持ちません。
以上によってグリシン以外のα-アミノ酸は、
すべて光学異性体を持ちます。
電気的性質
弱酸の-COOHと弱塩基の-NH2を持つことで、
陽イオンにも陰イオンにもなることができます。
特に両方が電離することで、
陽イオンかつ陰イオンである状態を「双性イオン」といいます。
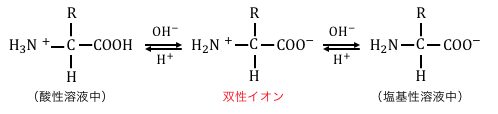
この図からも分かる通り、
H+の濃度が増せば平衡により-COOHが増え、
OH–の濃度が増せば-NH2が増えます。
このようにして酸性だと陽イオンが増し、
塩基性だと陰イオンが増します。
そして溶液全体で電荷のバランスが取れた状態を、
「等電点」といいます。
少し注意が必要なのは、
酸性アミノ酸や塩基性アミノ酸の場合です。
酸性アミノ酸は-COOHを2つ持つため、
すべてが双性イオンになっては電荷がマイナスです。
よってさらに強い酸性にすることで、
-COOHの電離を抑えることで等電点に達します。
以上のように等電点とは、
「すべてが双性イオンになるpH」ではなく、
「全体の電荷がバランスするpH」であることに注意しましょう。
ペプチド結合
-COOHと-NH2はアミド結合を作れるのでした。
-COOHと-NH2を両方持つアミノ酸は、
次々とつながることで高分子になることができます。
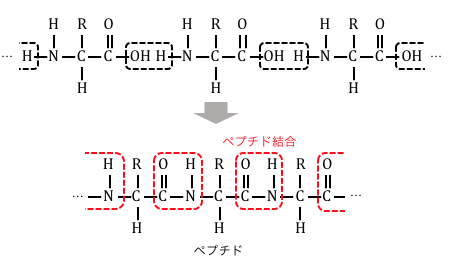
これによってできる高分子を「ペプチド」といいます。
また、このときのアミド結合を、
特別に「ペプチド結合」と呼びます。
アミノ酸の検出反応
次にアミノ酸の検出反応を見ていきます。
アミノ酸を検出する反応として、
①ニンヒドリン反応
②キサントプロテイン反応
③硫黄反応
④ビウレット反応
があります。
これらはごっちゃになりやすいので、
1つ1つ丁寧に確認していきましょう。
①ニンヒドリン反応
「ニンヒドリン反応」は、
α-アミノ酸の-NH2を検出して紫になる反応です。
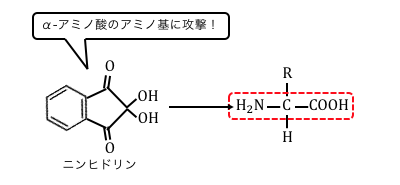
α-アミノ酸やペプチド、たんぱく質に、
ニンヒドリンを入れて温めることで、
紫色を呈色します。
どうでもいいですが、
ニンヒドリンってこうするとちょっと可愛いです。
余談はいいとして、
ニンヒドリン反応はα-アミノ酸があれば反応し、
紫色になるということをきっちり押さえておきましょう。
②キサントプロテイン反応
ベンゼン環を持つアミノ酸に反応して、
黄色を呈色するのが「キサントプロテイン反応」です。
アミノ酸の覚え方で勉強した通り、
ベンゼン環を持つアミノ酸は以下の通り。
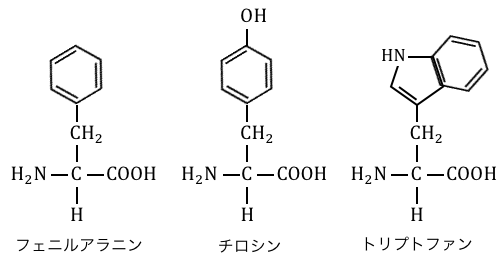
多くのたんぱく質にはこれらが含まれるため、
たんぱく質一般で反応を起こします。
ちなみにここで使う試薬は硝酸です。
手に硝酸がかかると黄色くなってしまいますが、
これはキサントプロテイン反応のせいなのです。
③硫黄反応
α-アミノ酸中の硫黄Sを検出して、
黒色沈殿を生じる反応が「硫黄反応」です。
硫黄を含むα-アミノ酸は以下の通り。
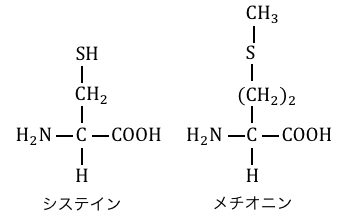
硫黄反応では、
まず固体NaOHを加えて加熱し、
そこに酢酸鉛を加えてPbS黒色沈殿を作ります。
④ビウレット反応
最後に一番厄介な検出反応である「ビウレット反応」です。
ビウレット反応では「2つ以上のペプチド結合」、
つまりトリペプチド以上を検出して、
赤紫色を呈色します。。
なぜこんなに中途半端な数なのかを確認しましょう。
ビウレット反応ではNaOHとCuSO4を加えることで、
2つのペプチド結合がCu2+に対して、
挟み込むように配位結合します。
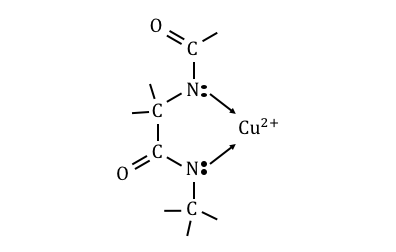
このような原理で起こるから、
2つ以上のペプチド結合=トリペプチド以上
という微妙な条件になるのです。
検出反応まとめ
以上の検出反応をまとめると以下の通り。
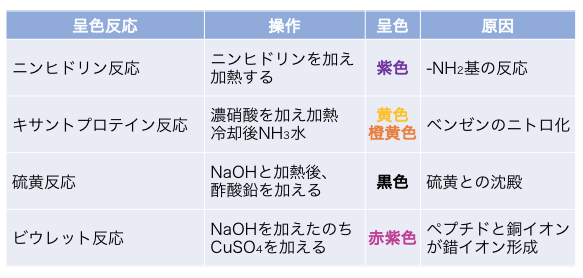
試験ではこれらの違いを問われるので、
確実に理解しておきましょう。
まとめ
今回はアミノ酸の性質の解説でした。
アミノ酸の基本的な性質と検出反応は理解できましたか?
この分野は高校3年生の最後に習うため、
演習不足で知識が曖昧になりがちです。
ぜひ何度か読み返して完璧な知識にしてください。














コメントを書く