今回はジアゾカップリングの解説です。
ジアゾ化とカップリングは、
ベンゼンがたくさん出てくるので構造式が大きくなります。
それを見ただけで、
「なんだこの反応!!??」
「絶対難しいよ!!!!」
と思い込んでしまう人が多いのです。
しかし冷静に反応の仕組みを追ってみれば、
ジアゾカップリングは全然難しくありません。
ここではジアゾカップリングについて、
その反応の仕組みから解説していきます。
ここの内容をしっかりと読めば、
ジアゾカップリングはもはやサービス問題と思えるでしょう。
しかも生成物の構造式が一見複雑なので、
有機化学が得意になった気持ちになれると思います。
そんな気持ちを味わってもらうために、
この記事の最後には「メチルオレンジの合成」の問題も用意しました。
ぜひ最後まで読んでいってくださいね。
ジアゾカップリングとは
「ジアゾカップリング」とは、
-N=N-というアゾ基を使ってベンゼン環を繋げる反応です。
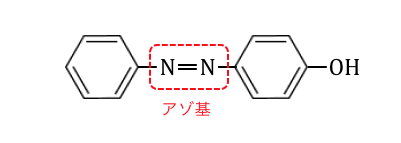
ジアゾカップリングの材料は「アニリン」です。
アニリンについては以下で詳しく解説しているので、
そちらも参考にしてみてください。
ジアゾカップリングの仕組み
ジアゾカップリングは主に、
「ジアゾ化」と「カップリング」の2段階に分けられます。
ベンゼン環がたくさんあるせいで、
とっても難しそうに見えてしまいますが、
仕組みを見ていけば意外とシンプルです。
それでは順番に確認していきましょう。
ジアゾ化
まずはアニリンを酸化してアゾ基の元を作ります。
ジアゾ化の材料はアニリンですが、
本当の主人公は実は「亜硝酸ナトリウム」です。
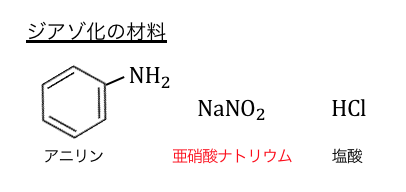
亜硝酸は非常に不安定な物質で、
普通にしていたらすぐに分解されてしまいます。
それをナトリウム塩にして形を留めたものが、
この亜硝酸ナトリウムです。
そんな不安定な亜硝酸ナトリウムに塩酸を加えると、
以下のように「ニトロソニウムイオンNO+」になります。
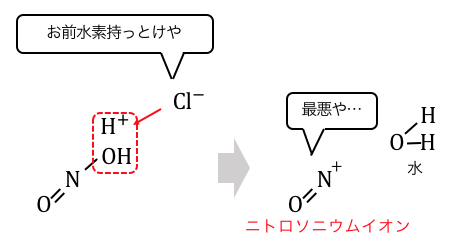
これはスルホン化やニトロ化で出てきたのと同じ仕組みですね。
この明らかに凶悪そうなNO+が、
アニリンの窒素を襲います。
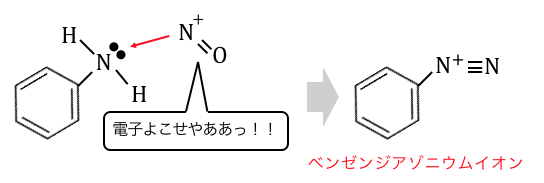
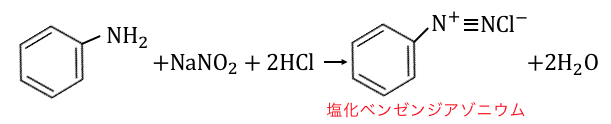
これによって「ベンゼンジアゾニウムイオン」ができました。
この-N+≡Nという構造がアゾ基の元になるのです。
以上を化学式で書くと以下です。
2つのHClによってNO+を作って反応しているイメージです。
王水を思い出してみるといいでしょう。
HNO3+3HCl→NOCl+Cl2+2H2O
ここでもNO+が現れています。N、O、Clは特別電気陰性度が高く、相性がいいのですね。
カップリング
このベンゼンジアゾニウムイオンに、
フェノール類や芳香族アミンを加えることで「カップリング」が起こります。
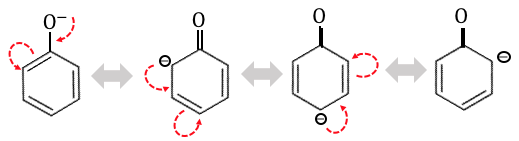
フェノールは以下のような「オルト-パラ配向性」があるのでした。
【合わせてチェック】
・フェノールの製法・性質・反応をどこよりも詳しく解説!
これによってフェノールは、
オルト位とパラ位が陰イオンのようになっているのです。
そんなフェノールが-N+≡Nに近づくことで、
カップリングが起こります。
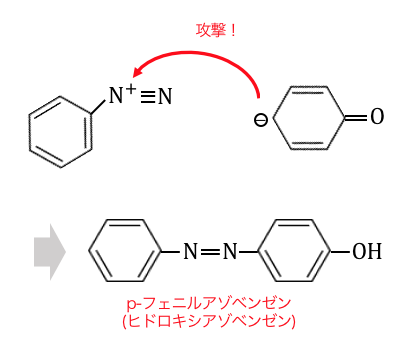
見た目は難しそうですが、
起こっていることはとっても単純でしたね。
オルト位は隣の-OHが邪魔で近づきにくく、パラ位の方が優先します。このように構造的に邪魔になるものを「立体障害」と言います。それに加えてナトリウム塩のときはオルト位よりパラ位の反応性が高くなるという理由もあります。
ジアゾカップリングの注意点
ベンゼンジアゾニウムイオンは不安定な物質です。
安定な窒素分子N2の状態から、
ベンゼン環に無理やり張り付かれているんだから、
そりゃ不安定ですよね。
よって高い温度では以下の加水分解によって、
フェノールと窒素に分解されてしまいます。
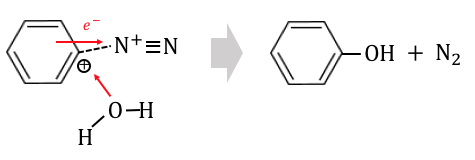
よってジアゾ化を行うときには、
0℃〜5℃という低温で行います。
ジアゾ化の主役NaNO2も不安定でしたから、
やはり低温の方が都合が良いですね。
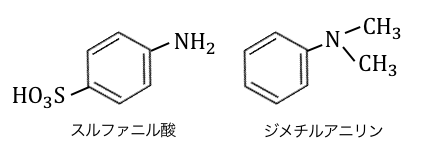
練習:メチルオレンジの合成
ジアゾカップリングは仕組みを理解した上で
一度自分で流れを追ってみると良いです。
今回は「メチルオレンジ」の合成をしてみましょう。
スルファニル酸に炭酸ナトリウムを加えて化合物Aとし、0℃で化合物Bと塩酸を加えて化合物Cにする。これにジメチルアニリンを加え、最後に水酸化ナトリウムを加えるとアゾ基を持つ化合物メチルオレンジが析出する。
(1)化合物A、B、Cはなにか。
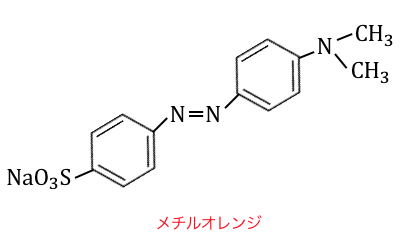
(2)メチルオレンジの構造式を求めよ。
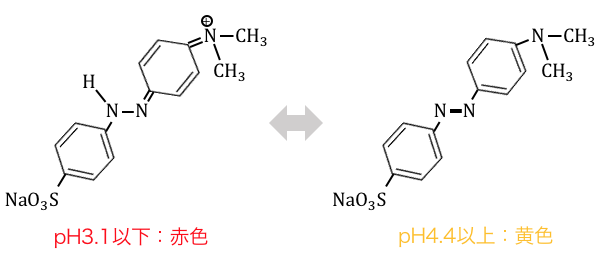
メチルオレンジといえば、
「中和滴定」で出てきた試薬です。
当たり前だけどメチルオレンジにも構造式があるんです。
なんかフラグ回収された感じでとってもワクワクしますね。
それでは解答です。
スルファニル酸はスルホ基を持っており酸性です。
一方炭酸ナトリウムは塩基性なので、
中和反応が起こって化合物Aが得られます。
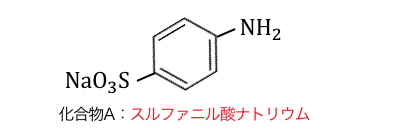
炭酸ナトリウムは弱酸由来の塩なので、
弱酸遊離と考えてもいいですね。
さて、ここに化合物Bを加えているわけですが、
最後に「アゾ基を持つ化合物」といっているので、
ここでジアゾ化をしているのでしょう。
ジアゾ化の主役は亜硝酸ナトリウムでしたから、
化合物BはNaNO2です。
これによって以下の反応が起こります。
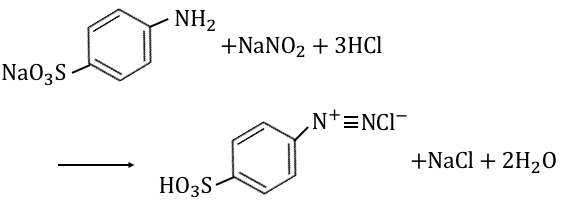
化合物Cは「塩化ベンゼンスルホン酸ジアゾニウム」ですね。
ここにジメチルアニリンを加えると、
カップリングが起こります。
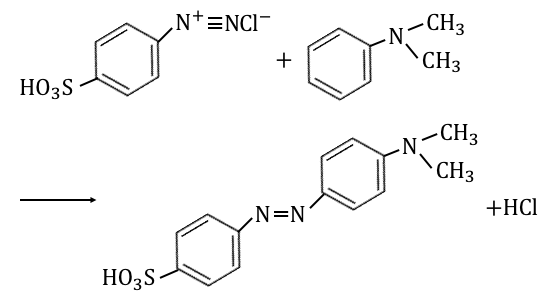
最後にスルホ基を中和してあげれば、
メチルオレンジの出来上がり!
まとめ
今回はジアゾカップリングの解説でした。
ジアゾ化は「亜硝酸ナトリウム」の力で、
アニリンの窒素が攻撃されて起こるのでした。
そしてカップリングでは、
「オルト-パラ配向性」と「立体障害」の影響で、
パラ位にカップリングが起こるのでしたね。
一見複雑な反応でも仕組みから理解すれば意外と簡単です。
聞いたことのある化合物を合成できる、
というのもなんだか楽しいですよね。
アニリンの反応はこのようにとても楽しいので、
得意科目にしてしまいましょう。














質問です
立体障害についてなのですが、オレンジIIはフェノール性ヒドロキシ基からみるとオルト位でカップリングしてますが、これは「例外」としてみて大丈夫ですか?それとも何か違う法則があるんですか??
コメントありがとうございます!
オレンジIIの場合はp位が潰れているので、
o位の方にカップリングしていると考えればいいと思います。
また今回は立体障害で説明しましたが、
官能基などの関係によっては全然例外もあると思います。
あくまで原則として見ておいてくださいー。