今回はエステルの解説です。
エステル化は有機化合物の構造決定で、
必ずと言っていいほど出てくる反応です。
大学入試において、
エステル化は絶対に押さえておかないといけません。
ここではエステル化を仕組みから解説します。
今まで丸暗記していたエステル化を、
とっても納得感を持って理解できるでしょう。
「エステル化って結局なに?」
「なんで加水分解なんかが起こるの?」
「酸でも塩基でも加水分解が起こるのはなんで?」
こんなもやもやもすっきり解決し、
どんな問題でも明確に解答できるようになります。
それでは解説していきましょう。
エステルとは

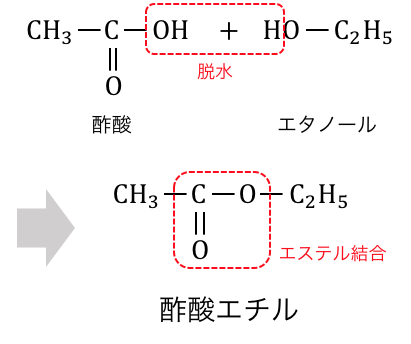
「エステル」とは、カルボン酸とアルコールが、
以下のように脱水されてできる物質です。
エステルは果物などの香りの成分です。
例えば先ほどの例で生じた「酢酸エチル」は、
りんごの香りの成分になっています。
少し親近感が湧きますね。
カルボン酸は-COOHがあることによって、
アルコールは-OHがあることによって水溶性でしたが、
エステルはそれらが結合してしまうので水に難溶です。
また同様に-COOHを失っているので中性ですね。
エステル化の仕組み
それではカルボン酸とアルコールが結びつく、
「エステル化」の仕組みを見ていきましょう。
まだカルボン酸とアルコールの性質が曖昧な人は、
以下を先にチェックしてみてくださいね。
それではエステル化を確認します。
カルボン酸の中のカルボニル基は、
電気陰性度の強い酸素が二重結合でくっついています。
そんな酸素のせいで、
以下のような状態になって反応性が高いのです。
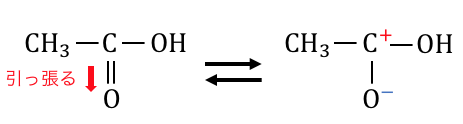
ここにアルコールの-OHが近づくことで反応が進みます。
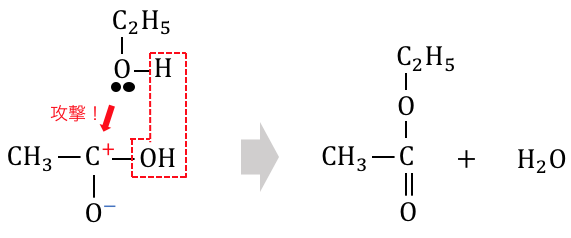
このようにしてエステルが完成しました。
ちなみにこの反応は可逆反応で、
エステル化の逆反応が「加水分解」です。
加水分解については次の章で説明します。
カルボニル基の酸素に水素を押し付けることで、反応しやすい状態にするためです。
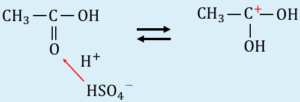
エステルの加水分解
先ほど言ったようにエステル化は可逆反応で、
逆反応のことを「加水分解」といいます。
加水分解の原理はエステル化と同じです。
硫酸が水素をぶつけて反応性が高まった炭素に、
水が攻撃することで反応が進みます。
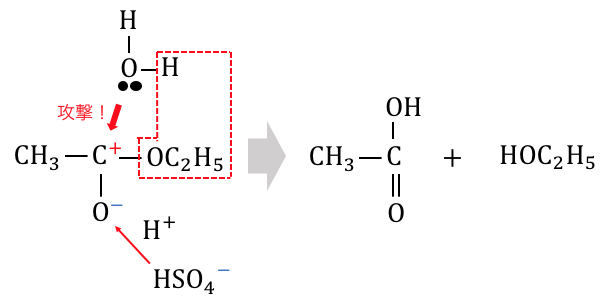
このときに硫酸と水が必要なので、
加水分解には「希硫酸」を用います。
参考:アセチル化とケン化
酢酸を分子間脱水した無水酢酸をぶつけることで、
酢酸エステルを作ることができます。
酢酸の一部の構造をアセチル基ということから、
この反応を「アセチル化」と呼びます。
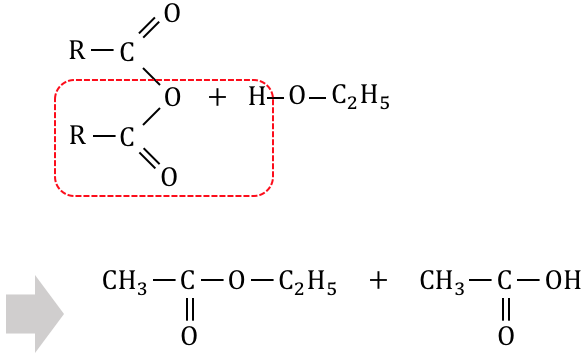
無水酢酸は非常に不安定なので、
この反応自体は不可逆反応です。
また、加水分解では陽性の炭素に水が反応しましたが、
強塩基を加えて熱することで、
より激しくエステルを分解することができます。
この反応を「ケン化」といいます。
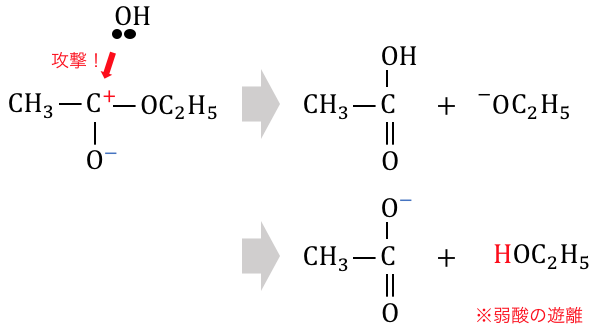
強塩基の力でどんどん-OHをぶつけて反応させるので、
この反応も不可逆反応になります。
まとめ
今回はエステルの解説でした。
エステルは、カルボン酸のカルボニル基に、
アルコールの-OHが攻撃をすることでできるのでした。
同じ仕組みでエステルに水が攻撃できるため、
エステル化は可逆反応なのでしたね。
エステル化は有機化学で最重要な反応と言っても
過言ではありません。
きっちりと仕組みから理解しておきましょう。














コメントを書く