今回はタンパク質の解説です。
タンパク質はあまり勉強する時間が取れず、
知識が曖昧になりがちです。
この記事では、
高校化学で必要なタンパク質の知識を、
網羅的に解説しています。
ぜひ一度目を通しておいてください。
目次
タンパク質とは
「タンパク質」とは、
アミノ酸がペプチド結合を繰り返すことでできる、
高分子化合物のことです。
アミノ酸の性質や覚え方に関しては、
以下の記事を参考にしてください。
タンパク質はたくさんのアミノ酸が繋がって
非常に複雑な構造をしています。
まずはその構造を確認していきましょう。
タンパク質の構造
①タンパク質の一次構造
タンパク質はペプチド結合で繋がるのでした。
このとき、アミノ酸がどの順で繋がっているか、
が「一次構造」です。
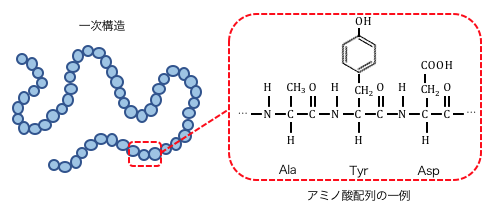
立体構造はとりあえず無視して、
順番だけに着目した構造です。
②タンパク質の二次構造
一次構造で繋がったタンパク質は、
ペプチド結合間で水素結合を作ります。
これによってできるのが「二次構造」です。
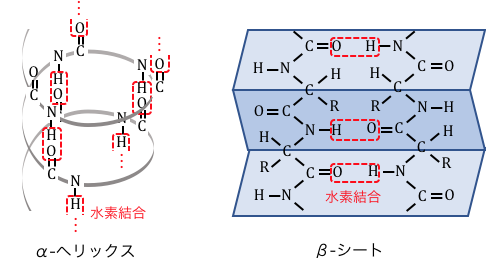
二次構造には、
右回りの螺旋構造を取る「α-ヘリックス」と、
平行に水素結合を作る「β-シート」があります。
③タンパク質の三次構造
二次構造を作ったタンパク質は、
さらに側鎖間の相互作用によって「三次構造」をとります。
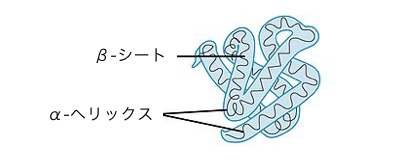
これによってα-ヘリックスやβ-シートが折りたたまれていきます。
④タンパク質の四次構造
タンパク質の中には、
三次構造を持ったもの同士が集まることで、
「四次構造」を作る場合があります。

例えば赤血球に含まれる「ヘモグロビン」は、
4つのタンパク質が四次構造を作っています。
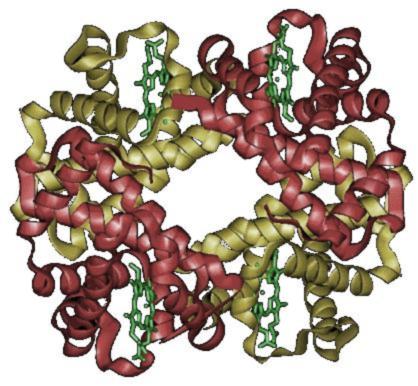
(参考:wiki-ヘモグロビン)
タンパク質の性質
タンパク質は20種類ものアミノ酸が関わり、
様々な二次構造、三次構造、四次構造を取るため、
構造によって多様な性質があります。
ここではタンパク質共通の性質に注目してみましょう。
①変性
タンパク質は複雑な構造になっているため、
熱や圧力、酸・塩基、重金属イオンなどによって、
立体構造が崩れて沈殿や凝固を起こします。
これをタンパク質の「変性」といい、
変性でタンパク質の機能を失うことを「失活」といいます。
変性を起こしたタンパク質は、
通常元の構造に戻ることができません。
②塩析
高分子化合物であるタンパク質は、
水溶液中で「親水コロイド」となります。
水素結合を作るペプチド結合が多いため、
親水性になりやすいのです。
これに多量の電解質を入れれば、
水和水が奪われて「塩析」を起こします。
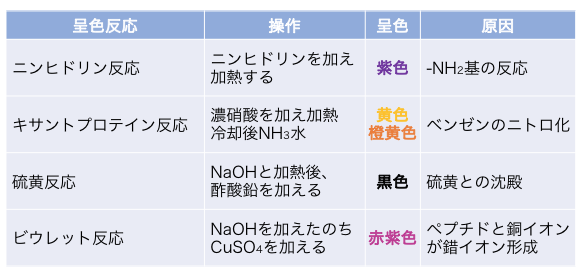
③呈色反応
アミノ酸がくっついてできたタンパク質は、
アミノ酸関連の以下の検出反応で呈色します。
タンパク質の分類
タンパク質には非常に多くの種類がありますが、
ここでは代表的なものだけを紹介しておきます。
まず最初の分類として、
α-アミノ酸だけからできるものを「単純タンパク質」、
糖、リン酸、色素、核酸などを含むものを「複合タンパク質」といいます。
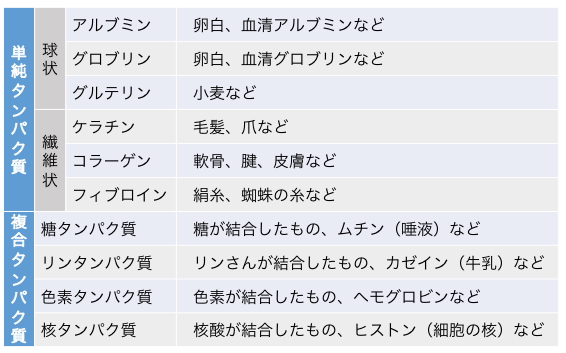
単純タンパク質はさらにその形から、
「球状タンパク質」と「繊維状タンパク質」に分けられます。
これらのうち有名なものを以下の表にまとめました。
まとめ
今回はタンパク質の性質を簡単にまとめました。
タンパク質自体はあまり出題されず、
アミノ酸関連の問題の方が多いです。
アミノ酸が不安な人はそちらも復習しておいてください。













コメントを書く